2021年12月1日,陕西麦科奥特科技有限公司全资子公司-西安奥立泰医药科技有限公司自主开发的1.1类新药MT2004获得国内临床试验批件,将开展I期桥接临床试验。目前,MT2004在已完成美国I期临床研究,即将进入临床II期研究,国际及国内临床进展顺利。
该药物用于治疗非酒精性脂肪性肝病(NAFLD)和其它相关肝病,非酒精性脂肪性肝病(NAFLD)是全球最常见的慢性肝病,疾病谱包括非酒精性肝脂肪变(NAFL)、非酒精性脂肪性肝炎(NASH)、肝硬化和肝细胞癌(HCC)。目前全球范围内还没有批准用于NAFLD/NASH的特异性药物。临床前研究数据表明:MT2004可降低肝纤维化、抑制NASH病程进展、降低血清转氨酶AST/ALT、改善肝损伤,且具有良好的安全性。美国I期临床试验证明了MT2004 对FXR受体的激动作用,未出现给药相关的严重不良反应、停药或出组,安全性十分良好;进一步在人体验证了MT2004早期设计的肝靶向作用,以及避免药物引起瘙痒和继发性肝功能损伤,有别于FXR其它在研药物如奥贝胆酸(OCA),MT2004没有出现瘙痒、肝酶升高等类似不良反应。预期未来会为广大肝病患者带来临床获益比更高的治疗方案。
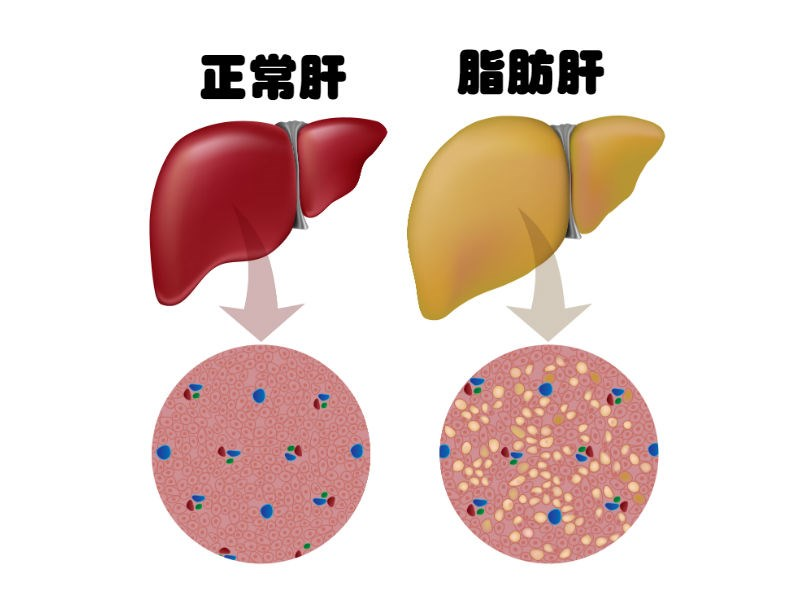
在全球范围内, NAFLD发病率大约为 25%,约3-5%的人患有NASH。在中国大约有2-3 亿NAFLD 患者,NASH 患者超过了3000万。截至目前,欧美日等规范性药品市场尚未批准可用于NASH治疗的新药。鉴于全球庞大患者人群中隐藏的医疗需求,德意志银行分析师曾做出预测,2025年全球NASH治疗药物的市场将达到350~400亿美元的规模,有望孕育出多款潜在重磅新药。 NASH治疗药物无论在中国还是全球医药市场,都有可观的市场前景和潜力。一旦有NASH的药物上市,临床需求巨大,MT2004国内临床试验的开展恰逢其时。

 企业邮箱
企业邮箱 企业OA
企业OA